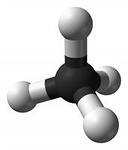
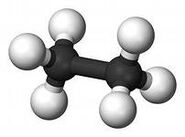
Углеводоро́ды — органические соединения, состоящие исключительно из атомов углерода и водорода. Углеводороды считаются базовыми соединениями органической химии, все остальные органические соединения рассматривают как их производные. Поскольку углерод имеет четыре валентных электрона, а водород — один; простейший углеводород — метан имеет формулу (CH4).
При систематизации углеводородов принимают во внимание строение углеродного скелета и тип связей, соединяющих атомы углерода. В зависимости от строения углеродного скелета углеводороды подразделяют на ациклические и карбоциклические. В зависимости от кратности углерод-углеродных связей углеводороды подразделяют на предельные (алканы) и непредельные (алкены, алкины, диены). Циклические углеводороды разделяют на алициклические и ароматические.
|
Ациклические (с открытой цепью) |
Карбоциклические (с замкнутой цепью) | ||||
|---|---|---|---|---|---|
|
предельные |
непредельные |
предельные |
непредельные | ||
|
с одинарной связью |
с двойной связью |
с тройной связью] |
с двумя двойными связями |
с одинарной связью |
с бензольным кольцом |
|
ряд метана (алканы) |
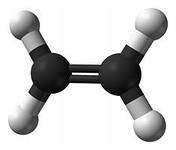
ряд этилена (алкены) |
ряд ацетилена (алкины) |
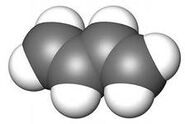
ряд диеновых углеводородов |
ряд полиметиленов (нафтены) |
ряд бензола (ароматические углеводороды, или арены) |
Углеводороды, как правило, не смешиваются с водой, поскольку атомы углерода и водорода имеют близкую электроотрицательность, и связи в углеводородах малополярны. Для предельных углеводородов характерны химические реакции замещения, а для непредельных — присоединения.
Основные источники углеводородов — нефть, природные газы и каменный уголь.
Сравнительная таблица углеводородов[]
|
Характеристика |
Алканы |
Алкены |
Алкины |
Алкадиены |
Циклоалканы |
Арены |
|---|---|---|---|---|---|---|
|
Общая формула |
CnH2n+2 |
CnH2n |
CnH2n-2 |
CnH2n-2 |
CnH2n |
CnH2n-6 |
|
Строение |
sp³-гибридизация — 4 электронных облака направлены в вершины тетраэдра под углами 109°28'. Тип углеродной связи — σ-связи |
sp²-гибридизация, валентный угол 120°.Тип углеродной связи — π-связи. lc-c — 0,134 нм. |
sp-гибридизация, молекула плоская (180°), тройная связь, lc-c — 0,120 нм. |
lc-c — 0,132 нм – 0,148 нм, 2 или более π-связей. У каждого атома три гибридные sp²-орбитали. |
sp³-гибридизация, валентный угол около 100° lc-c — 0,154 нм. |
Строение молекулы бензола (6 р-электронов, n = 1), Валентный угол 120° lc-c — 0,140 нм, молекула плоская (6 π | σ) |
|
Изомерия |
Изомерия углеродного скелета, возможна оптическая изомерия |
Изомерия углеродного скелета, положения двойной связи, межклассовая и пространственная |
Изомерия углеродного скелета, положения тройной связи, межклассовая |
Изомерия углеродного скелета, положения двойной связи, межклассовая и цис-транс-изомерия |
Изомерия углеродного скелета, положения двойной связи, межклассовая и цис-транс-изомерия |
Изомерия боковых цепей, а также их взаимного положения в бензольном ядре |
|
Химические свойства |
реакции замещения (галогенирование, нитрирование), окисления, радикальное галогенирование CH4 + Cl2 → CH3Cl + HCl (хлорметан), горения, отщепления (дегидрирование) |
Реакции присоединения (гидрирование, галогенирование, гидрогалогенирование, гидратация), горения |
Реакции присоединения (гидрирование, галогенирование, гидрогалогенирование, гидратация), горения |
Реакции присоединения |
Для колец из 3-4 атомов углерода - раскрытие кольца |
Реакции электрофильного замещения |
|
Физические свойства |
С CH4 до C4H10 — газы; с C5H12 до C16H34 — жидкости; после C17H36 — твёрдые тела. |
С C2H4 до C4H8 — газы; с C5H10 до C17H34 — жидкости, после C18H36 — твёрдые тела. |
Алкины по своим физическим свойствам напоминают соответствующие алкены |
Бутадиен — газ (t кип −4,5 °C), изопрен — жидкость, кипящая при 36 °C, диметилбутадиен — жидкость, кипящая при 70 °C. Изопрен и другие диеновые углеводороды способны полимеризоваться в каучук |
С C3H6 до C4H8 — газы; с C5H10 до C16H32 — жидкости; после C17H34 — твёрдые тела. |
Все ароматические соединения — твердые или жидкие вещества. Отличаются от алифатических и алициклических аналогов высокими показателями преломления и поглощения в близкой УФ и видимой области спектра |
|
Получение |
Восстановление галогенпроизводных алканов, восстановление спиртов, восстановление карбонильных соединений, гидрирование непредельных углеводородов, Реакция Вюрцa. |
Каталитический и высокотемпературный крекинг углеводородов нефти и природного газа, реакции дегидратации соответствующих спиртов, дегидрогалогенирование и дегалогенирование соответствующих галогенпроизводных |
Основным промышленным способом получения ацетилена является электро- или термокрекинг метана. Пиролиз природного газа и карбидный метод. |
Постадийное дегидрирование алканов, дегидрирование спиртов. |
Гидрирование ароматических углеводородов, отщепление двух атомов галогена от дигалогеналканов |
Дегидрирование циклогексана, тримеризация ацетилена, выделение из нефти |
| ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||